GAMP - przepisy, walidacja

A. Łobzowski, W. Szkolnikowski
LAB-EL Elektronika Laboratoryjna S.J.
Artykuł publikowany w piśmie POMIAR nr 4/2009
Co firma LAB-EL ma do powiedzenia w tematyce GAMP 4 - cz. 1
W kilku artykułach zamieszczonych w 2006 r na łamach pisma Pomiar, opisywaliśmy systemy do monitoringu parametrów środowiskowych w pomieszczeniach magazynów i hurtowni oraz w środkach transportu, wymaganych w procesach produkcji i dystrybucji wyrobów farmaceutycznych i spożywczych. Ze względów oczywistych, ostrzejsze obostrzenia prawne dotyczą produktów farmaceutycznych. Obowiązujące w Polsce dokumenty prawne dotyczące omawianego zagadnienia to: Ustawa z dnia 6.09.2001 Prawo Farmaceutyczne (Dz.U.08.45.271) oraz Rozporządzenie Ministra Zdrowia z dnia 1.10.2008 w sprawie wymagań Dobrej Praktyki Wytwarzania (GMP) (Dz.U.08.184.1143 z dnia 17.10.2008). Szczególnie dokument dotyczący wymagań GMP, definiuje pewne pojęcia, jakie będą omawiane w dwuczęściowym artykule poświęconym zagadnieniom kwalifikacji systemów skomputeryzowanych oraz ich walidacji. W części pierwszej opiszemy wymagania dotyczące realizacji owych zagadnień, w drugiej natomiast przedstawimy ofertę firmy LAB-EL w konkretnych ich zastosowaniach.
Każdy przepis prawa zawiera skrótowy, zwięzły opis zagadnienia, dlatego jego interpretacja jest czasem dość trudna. Z tego powodu powstało wiele przewodników będących próbą interpretacji owych przepisów w warunkach przemysłowych. Podstawowym przewodnikiem dotyczącym walidacji systemów skomputeryzowanych jest GAMP 4.0, a ostatnio zmodyfikowany GAMP 5.0.
Systemy zautomatyzowane i skomputeryzowane stosowane szczególnie w przemyśle wysokich technologii, do którego należy farmacja, w świetle omówionych przepisów prawa muszą być poddawane okresowym sprawdzeniom potwierdzającym ich jakość w celu wykrycia ewentualnych potencjalnych zagrożeń wynikających z bezpośredniego lub pośredniego wpływu na produkt końcowy. Walidacja zatem ma udokumentować w jaki sposób należy zmienić i/lub udoskonalić proces, aby zminimalizować ewentualne skutki jego nieprawidłowego działania. W tym celu warto przeprowadzić analizę wpływu i analizę ryzyka. Zgodnie z definicjami zacytowanymi na podstawie dokumentu dotyczącego wymagań GMP:
- analiza ryzyka (RA – Risk analysis) - metoda oceny i opisu parametrów krytycznych dla funkcjonowania wyposażenia lub procesu;
- kwalifikacja (Q – Qualification) - działanie mające na celu wykazanie i udokumentowanie, że urządzenia lub instalacje pomocnicze są odpowiednio zainstalowane, pracują właściwie, a ich działanie rzeczywiście prowadzi do uzyskania oczekiwanych wyników; kwalifikacja jest częścią walidacji, lecz poszczególne, pojedyncze etapy kwalifikacji nie stanowią procesu walidacji;
- kwalifikacja instalacyjna (IQ – Installation Qualification) - udokumentowana weryfikacja stwierdzająca, że obiekty, systemy i urządzenia, zainstalowane lub zmodyfikowane, są zgodne z zatwierdzonym projektem i zaleceniami producenta;
- kwalifikacja operacyjna (OQ – Operational Qualification) - udokumentowana weryfikacja stwierdzająca, że obiekty, systemy i urządzenia, zainstalowane lub zmodyfikowane, funkcjonują tak, jak zamierzono w przewidywanych zakresach operacyjnych;
- kwalifikacja procesowa (PQ – Performance Qualification) - udokumentowana weryfikacja stwierdzająca, że obiekty, systemy i urządzenia, jako całość, działają skutecznie i w sposób powtarzalny w odniesieniu do zatwierdzonego procesu i specyfikacji produktu;
- kwalifikacja projektu (DQ - Design Qualification) - udokumentowana weryfikacja stwierdzająca, że proponowany projekt obiektów, systemów i urządzeń jest odpowiedni do zamierzonego celu;

Systemy skomputeryzowane (def: system skomputeryzowany - proces lub operacja zintegrowana z systemem komputerowym), według GAMP 4.0 podzielono na pięć kategorii oprogramowania i dwie kategorie sprzętu. Podział ten pomaga w ustaleniu koncepcji walidacji w zależności od rzeczywistego zagrożenia wnoszonego przez system skomputeryzowany. Tak więc, podział oprogramowania przedstawia się następująco:
- kategoria 1 – systemy operacyjne, oprogramowanie sieciowe (Systemy operacyjne są platformami działania oprogramowania aplikacyjnego, stąd ich walidacja jest równoczesna z walidacją aplikacji);
- kategoria 2 – standardowe instrumenty pomiarowe (Należą do nich wszystkie przyrządy pomiarowe zawierające firmware, na funkcje którego użytkownik nie ma wpływu, może jedynie zmieniać parametry konfiguracyjne);
- kategoria 3 – standardowe pakiety oprogramowania (Pakiety wspomagające prace biurowe, edytory tekstów, bazy danych, arkusze kalkulacyjne, itp. O ile sam pakiet np. MS Excel można uznać za zwalidowany, o tyle formuły matematyczne tworzone przez użytkownika muszą podlegać walidacji);
- kategoria 4 – konfigurowalne pakiety oprogramowania (Oprogramowanie typu SCADA w tym oferowany przez LAB-EL program LBX – systemy te umożliwiają użytkownikowi tworzenie własnych aplikacji przez wykorzystanie zdefiniowanych bloków funkcjonalnych (funktorów). W tym przypadku należy przeprowadzić analizę wpływu na proces oraz analizę ryzyka. W oparciu o wyniki analizy należy opracować plan walidacji uwzględniający szczegółowo zakres poszczególnych testów kwalifikacyjnych, w tym przegląd kodu źródłowego);
- kategoria 5 – oprogramowanie dedykowane (Oprogramowanie tej kategorii jest tworzone dla określonego użytkownika lub grupy użytkowników. Walidacja tego typu oprogramowania powinna objąć cały cykl życia systemu (def: cykl życia systemu – planowanie, specyfikowanie, projektowanie, konstruowanie, testowanie, instalacja w środowisku docelowym, odbiór i akceptacja, użytkowanie, wycofanie systemu z eksploatacji).
Podział sprzętu przedstawia się następująco:
- kategoria 1 – systemy typowe (należą tu np.: stacje robocze, drukarki, standardowe peryferia, sprzęt sieciowy, itp. Kwalifikacja instalacyjna ograniczona być może tylko do identyfikacji elementów systemu).
- kategoria 2 – systemy dedykowane (zalicza się tutaj sprzęt dedykowany do konkretnego zastosowania. W tym przypadku zalecane jest wykonanie pełnych testów obejmujących kwalifikację IQ, OQ, oraz PQ dla całego systemu).
Przewodnik GAMP przedstawia cykl życia systemu w
powiązaniu z jego walidacją. Standardowy model przebiegu procesu zwany
modelem „V”, polega na „wędrówce systemu” po linii litery V począwszy
od jej lewego górnego rogu, a kończy drogę w prawym górnym rogu linii.
Cykl życia systemu wg modelu „V”, przedstawia poniższy rysunek:
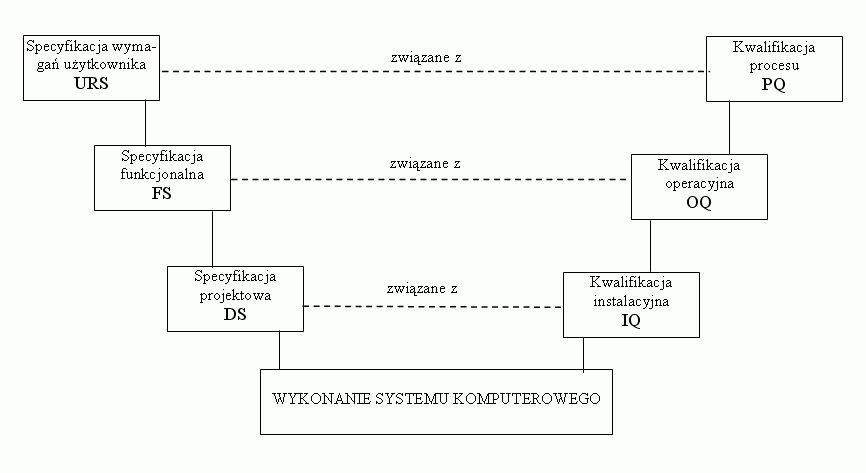
W następnym numerze magazynu Pomiar przedstawimy dalsze wymagania przewodnika GAMP oraz opiszemy w jaki sposób firma LAB-EL realizuje kwalifikację swoich skomputeryzowanych systemów instalowanych w zakładach i hurtowniach przemysłu farmaceutycznego.
 Hurtownie farmaceutyczne
Hurtownie farmaceutyczne
 Łańcuch chłodniczy dostaw
Łańcuch chłodniczy dostaw

 | tel. +48 22 753 61 30 | fax +48 22 753 61 35
| tel. +48 22 753 61 30 | fax +48 22 753 61 35